En el cultivo del anturio y de la Phalaenopsis hay que prestar mucha atención a los niveles de acidez. La acidez, o valor de pH, es una escala logarítmica que indica el número de iones H+. El agua con un pH neutro de 7 tiene tantos iones H+ como iones OH-. Un pH inferior a 7 es ácido y un pH superior a 7 es básico (alcalino). La escala es logarítmica, lo que significa que un pH de 6 es diez veces más ácido que un pH de 7.
El valor del pH es importante para la absorción de varios elementos nutritivos, ya que si el pH es muy alto o muy bajo ciertos nutrientes no se absorben de modo adecuado. Tanto para el anturio como para la Phalaenopsis, el pH óptimo está entre 5 y 6. Con un pH alto, sustancias como el boro, los fosfatos y el cobre se absorben con dificultad. Con un pH bajo, se dificulta la absorción del nitrógeno, del molibdeno y del azufre. A un pH extremadamente bajo, pueden presentarse también síntomas de intoxicación debido, por ejemplo, al manganeso o al aluminio.
| Difícil o imposible de absorber a un pH <5 | Difícil o imposible de absorber a un pH >6 |
| Nitrógeno (N) | Boro (B) |
| Molibdeno (Mo) | Fosfatos (P) |
| Azufre (S) | Cobre (Cu) |
Agua de riego
Cuando se utiliza agua de lluvia u osmotizada, el agua contiene muy pocas sustancias en disolución. El agua de riego y del grifo contienen de forma natural bicarbonato, que ejerce un efecto tampón del pH. El agua de lluvia presenta un pH de alrededor de 6,5 pero, al no contener una sustancia tampón, puede sufrir con rapidez cambios en su pH, por lo que se aconseja añadirle bicarbonato. Una dosis apropiada es de 36g/m3 ,que suponen unos 0,35 mmol de HCO-3.
Dependiendo del pH del agua de partida y, posiblemente, de la de recirculación, el agua de riego se acidifica o alcaliniza mediante un regulador del pH. Es importante incluir una cantidad suficiente de ácido o álcali en el programa de fertilización. Si aún así el pH sigue necesitando muchos ajustes, puede ser que el ácido o el álcali no hayan actuado por completo antes de que el agua alcance el sensor de pH. Hay que tener cuidado con esto para no añadir demasiado ácido o álcali.
Por todo esto hay que medir el pH del agua de riego de las tuberías al menos una vez al mes. El momento adecuado es después de limpiar por completo los conductos para que no quede agua estancada de la sesión de riego anterior. Este aspecto es particularmente significativo si el suministro de agua no es diario. Con un suministro diario, el agua de riego se estanca un tiempo y los fertilizantes tienen tiempo de reaccionar. Lo habitual es regular el pH del suministro diario mediante la adición de un ácido o álcali antes de que el agua llegue al invernadero.
Tanques de fertilización
Para que los fertilizantes puedan disolverse en el tanque, es esencial que el pH no exceda de 6. Aconsejamos mantener un pH entre 4 y 5 para que todas las sustancias se disuelvan correctamente. También es fundamental que el hierro no coincida en el mismo recipiente con el ácido fosfórico y el ácido nítrico: los ácidos atacan los quelatos de hierro, con lo que el hierro se oxida, el Fe3+ absorbible se une al O2 y se convierte en Fe2O3 no absorbible (óxido).
Acidez del sustrato
El pH del sustrato suele ser diferente al del agua de riego o de drenaje. Esto se debe a dos procesos: la absorción de nutrientes por parte de la planta y la transformación de los fertilizantes por parte de los organismos presentes en el suelo.
El primer proceso es el de mayor impacto. La carga eléctrica de la planta debe permanecer neutra; esto significa que si la planta absorbe, por ejemplo, potasio (K+), liberará hidrógeno (H+). Por otro lado, también quiere decir que, si la planta absorbe, por ejemplo, nitrato (NO3–), liberará hidróxido (OH–). Si los cationes (iones de carga positiva) y los aniones (iones de carga negativa) se absorben por igual, el pH del sustrato no varía. En este caso, el H+ liberado por la planta se unirá al OH– para formar agua (H2O). Si no hay un equilibrio entre el H+ y el OH–, el pH variará.
Dado que las raíces de las plantas respiran, se produce CO2 en el sustrato. Cuando hay OH– libre, este reaccionará con el CO2 para formar bicarbonato (HCO3-). Si se absorben aniones, aumenta el pH del sustrato.
Influencia de los organismos del suelo
Los organismos del suelo convierten en nitrato los fertilizantes que contienen amonio. Este proceso se denomina nitrificación, y se desarrolla según la reacción siguiente:
NH4 + 2 O2 -> NO3 + 2H+ + H2O
En este proceso se libera H+, que ejerce un efecto acidificante. Si se emplea urea, esta se transforma primero en amonio mediante la ureasa, según la reacción siguiente:
![]()
Esta reacción aumenta un poco el pH porque el amoníaco es alcalino. No obstante, tras esta reacción también tiene lugar la nitrificación del amoníaco, por lo que se libera de nuevo H+. Por lo tanto, la urea neta también ejerce un efecto acidificante.
Durante el crecimiento generativo, se absorbe más potasio que durante el crecimiento vegetativo. A medida que la planta envejece, se libera más H+ y el pH disminuye.
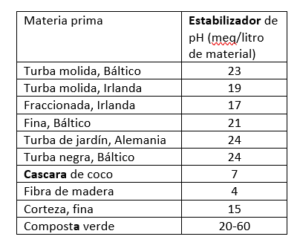
Para contrarrestar las fluctuaciones del pH, hay que tamponar el sustrato con frecuencia. Sin embargo, los sustratos difieren en cuanto a su capacidad tampón: la turba, por ejemplo, tiene una mayor capacidad tampón que la médula de coco. El volumen del tampón se indica en meq o mmol por litro. Los sustratos con un bajo tampón de pH ofrecen menos capacidad de compensar las fluctuaciones y, por tanto, reaccionan de forma más impredecible. El tampón también deja de hacer efecto con el tiempo, por lo general tras 8-12 semanas.
El pH y la Phalaenopsis
Medidas a adoptar
En la Phalaenopsis, la acidificación del sustrato es un proceso natural; durante las fases de inducción y de terminación, el pH puede disminuir de forma drástica. Las fluctuaciones del pH, por ejemplo durante el riego, pueden provocar causar el ennegrecimiento de las puntas radiculares.

Mala calidad de las raíces de la Phalaenopsis.
Estas raíces dañadas son puntos por donde el Fusarium y el Pythium pueden penetrar en la planta. Por eso es fundamental compensar las fluctuaciones de pH en el sustrato. Para ello pueden adoptarse diversas medidas:
Añadir cal al sustrato
Al comenzar el período de cultivo pueden añadirse unos 3kg/m3 de Dolokal. El Dolokal contiene carbonato de calcio, carbonato de magnesio y óxido de magnesio, sustancias que la cal en polvo va liberando durante el cultivo. En un entorno ácido, el carbonato absorberá los iones H+, lo que evita la disminución del pH. El inconveniente del Dolokal es que sustratos gruesos, como la corteza, lo eliminan con bastante rapidez. Por eso es especialmente activo durante las primeras semanas.
Reducir el amonio y la urea
Como se ha descrito anteriormente, la nitrificación del amonio libera H+, que ejerce un efecto acidificante. El H+ también se excreta cuando la planta absorbe NH4–. Por este motivo el nitrógeno amoniacal suele sustituirse por nitrógeno nítrico cuando el pH del sustrato disminuye. Si se utilizan fertilizantes líquidos, la administración de amonio puede reducirse a 0 mmol en caso necesario. Cuando se emplean fertilizantes sólidos como el nitrato de calcio, siempre habrá presente cierta cantidad de amonio; el valor más bajo que se puede alcanzar es de unos 0,25 mmol de amonio. Los fertilizantes mixtos como el PG-mix y el Osmocote también contienen una moderada cantidad de amonio.
Lavar con agua limpia
SI el sustrato no está bien lavado, se acumulan los fertilizantes y los exudados de las raíces. Esto suele producir una disminución del pH. Para restablecerlo a valores apropiados, hay que diluir estas sustancias del sustrato lavándolo con agua limpia que esté a un pH aproximado de 6,5.

Buena calidad de la raíz en Phalaenopsis.
El pH y el anturio
Por norma general, el anturio se desarrolla mejor con un pH bajo. Con un pH superior a 6,2, sus hojas y flores pierden el brillo con rapidez debido a un crecimiento deficiente. Si además se administran cantidades elevadas de calcio (Ca++) y de bicarbonato (HCO3), el cultivo se contamina por la precipitación de carbonato de calcio (CaCO3).

Contaminación foliar por carbonato de calcio (CaCO3).
El pH del anturio varía según la estación del año. En primavera, el pH suele incrementarse debido al aumento del crecimiento natural. La planta absorbe más NO3- durante este período, lo que incrementa su pH. En cambio, en otoño se absorben más iones de carga positiva como el K+ y el Ca++, lo que disminuye el pH. El uso de fertilizantes que contienen amonio también puede tener un efecto significativo de reducción del pH. Esto ocurre especialmente en invierno, cuando se suministra una mayor cantidad de nitrato de calcio sólido. El aporte de amonio (NH4+) puede llegar a ser entonces de hasta 0,5-0,7 mmol/l, lo que ejerce un fuerte efecto acidificante. En este caso, se recomienda optar por el nitrato de calcio líquido, ya que no contiene NH4+.
Durante el cultivo, el pH disminuye y, por tanto, el agua de drenaje suele presentar un pH bajo. Si para regar se utiliza una alta proporción de agua de drenaje, puede ser necesario volver a corregir el pH.
Un pH bajo aumenta la desprotección de las flores frente a fenómenos como la decoloración azul y la vidriosidad.

Decoloración azul en las brácteas.
Anturio de maceta
En el caso del anturio de maceta, los valores de pH en la maceta no suelen fluctuar porque el cultivo se realiza en sustratos orgánicos y en un período relativamente breve. Para lograr que al inicio del cultivo el pH sea neutro (alrededor de 5,6-5,8) a los sustratos de turba se les añade cal (suele emplearse el Dolokal). Sin embargo, la conjunción de agua de pozo con un sustrato alcalino puede disparar los valores de pH. Un pH excesivamente elevado entorpece la absorción de oligoelementos y esto puede reducir el brillo de la planta. Para evitarlo, hay que mantener un pH en la maceta entre 5,2 y 5,8.
Anturio de flor cortada
La trayectoria de los valores de pH de un cultivo de anturio de flor cortada se ve influida por tres factores:
– control de la variedad
– influencias del sustrato
– el pH del agua de riego
Control de la variedad
Qué variedad en concreto se cultiva puede influir sobremanera en el pH del sustrato o del agua de drenaje. Debido a la absorción selectiva de elementos, en las especies más delicadas (Moments®, Acropolis® y Angel®) el pH puede desplomarse y alcanzar valores muy bajos. No es raro observar pHs de de 2,0.

Valor bajo de pH en un pH-metro.
Influencia del sustrato
El sustrato en el que crece la planta influye de modo significativo en el pH del entorno radicular y del agua de drenaje. En el caso de la lana de roca, el pH suele mantenerse alto, mientras que con la perlita el pH del agua de drenaje puede disminuir considerablemente después de 6-9 meses de cultivo. El oasis ya es de por sí ácido, pero desde el principio se le añade cal con Dolokal/Dolomita.
Agua de riego
Los cultivadores que usan agua de manantial como agua de partida no suelen tener problemas de pH excesivamente bajo; sino que más bien son de pH demasiado alto.
pH en el entorno radicular/agua de drenaje
Por norma general, el pH del sustrato es mayor que el del agua de drenaje, con una diferencia del orden de 1-2 puntos. Así, con un pH de 4,0 en el agua de drenaje, en el entorno radicular puede llegar a ser de 5,0 e incluso superior.
Debido al prolongado tiempo de cultivo del anturio de flor cortada, el pH en el entorno de la raíz y del agua de drenaje puede acabar alcanzando valores muy bajos. No hay motivos para preocuparse mientras el pH no baje de 3,0 en el agua de drenaje. Sin embargo, hay que evitar que descienda de este valor, ya que puede producirse un daño directo en las raíces y acabarían muriendo en solo unas pocas semanas. Este fenómeno se denomina reducción radicular.

Reducción radicular debido a un pH muy bajo en el entorno de las raíces.







